近日,我校生命科学学院金丽华科研团队的研究成果取得新进展,相关论文“Atg2 coordinates microbial metabolite signaling and epigenetic remodeling to maintain intestinal lipid homeostasis in Drosophila”在国际知名期刊Microbiome(中科院一区,影响因子IF = 12.7)正式发表。这一成果为肠道代谢紊乱相关疾病的防治提供了全新理论依据与潜在治疗靶点,充分彰显了我校在生命科学领域的高水平学术创新能力。

肠道稳态失衡与肥胖、非酒精性脂肪肝以及炎症性肠病等多种代谢性疾病息息相关,而自噬相关蛋白Atg2在肠道代谢调控中的具体作用机制长期以来未能被完全阐明。该研究以果蝇为模式生物,综合运用组织特异性基因操作、多组学分析及微生物干预等多重实验手段,首次揭示了Atg2的全新功能,通过调控肠道微生物群、微生物代谢物短链脂肪酸(SCFA)与表观遗传修饰的协同作用,精准维持肠道脂质代谢与肠道免疫稳态。
研究深入剖析了背后的分子通路:Atg2缺失会导致果蝇肠道自噬流异常,进而引发肠道菌群失调,促使短链脂肪酸过量产生。过量的短链脂肪酸将造成乙酰辅酶 A 积累,引发蛋白质广泛超乙酰化,最终激活脂肪生成程序并启动先天免疫反应,导致肠道脂质积累、免疫功能紊乱乃至果蝇寿命缩短。此外,研究证实组蛋白去乙酰化酶HDAC3是介导这一调控过程的关键分子;而膳食组氨酸补充可通过调节肠道菌群与HDAC3表达,有效逆转Atg2缺失引发的代谢紊乱,为相关疾病的营养干预提供了新的思路。
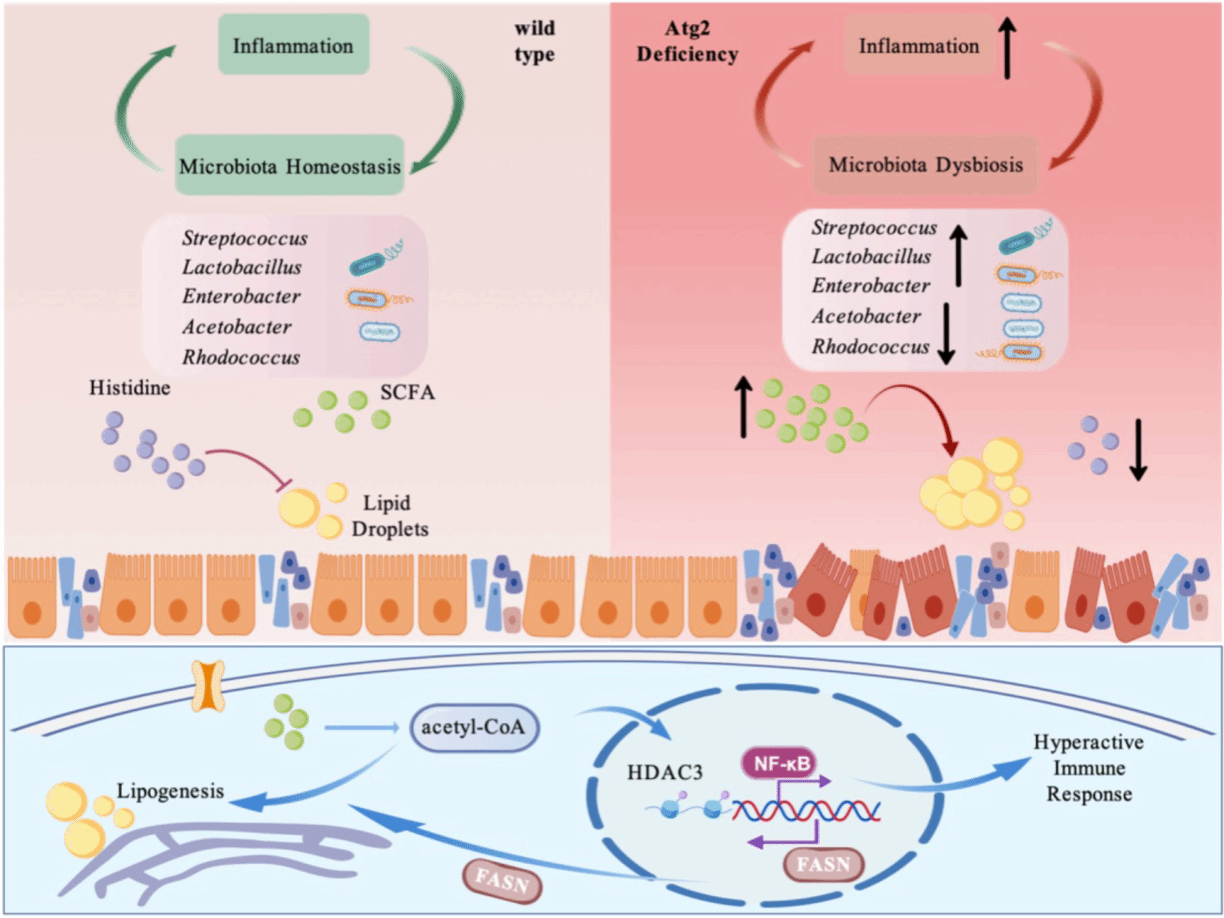
Atg2维持肠道干细胞和肠道菌群稳态的分子机制
本研究的核心创新点在于首次系统构建了Atg2 - 肠道微生物 -短链脂肪酸- 表观遗传的调控轴,明确了Atg2在肠道微生物与宿主代谢互作中的核心整合作用,打破了以往将Atg2仅视为自噬相关蛋白的传统认知,丰富了肠道稳态调控的分子机制理论体系。该成果不仅填补了自噬、肠道微生物与表观遗传交叉领域的研究空白,更为肥胖、非酒精性脂肪肝以及炎症性肠病等代谢性疾病的治疗提供了新靶点与新策略,具备重要的学术价值与广阔的临床转化潜力。
论文第一作者为我校博士研究生王平,由金丽华教授指导。相关原始测序数据已上传至中国国家生物信息中心基因组序列归档库(GSA),面向全球科研工作者共享开放。
论文连接:https://link.springer.com/article/10.1186/s40168-026-02356-2#Abs1
视频连接:http://xhslink.com/o/9stdl3gZpRW